(Este post es una adaptación de un post escrito por Alfons-Nonell, CEO y co-fundador de DevsHealth.)
La teoría del cisne negro o teoría de los sucesos del cisne negro es una metáfora que describe un suceso sorpresivo (para el observador), de gran impacto socioeconómico. Es una teoría creada por Nassim Taleb y que explicó en su libro homónimo de El Cisne Negro.
Posteriormente, tomando la figura del cisne negro como un evento inesperado y con un impacto extremo en la economía y las finanzas, el Bank for International Settlements (BIS) lanzó el concepto de cisne verde en febrero de 2020. El cisne verde hace referencia a una posible crisis financiera provocada por el cambio climático, teniendo en cuenta las graves consecuencias que éste podría ocasionar a nivel mundial.
Pues, bien siguiendo con la metáfora de los cisnes, toca ‘El cisne rojo’ metáfora de una enorme problema de salud mundial que se avecina.
Que viene el Cisne Rojo
Escribe Alfons Nonell de DevsHealth que el 19 de enero, The Lancet publicó un artículo que contiene un análisis sistemático de la carga mundial de resistencia bacteriana en 2019. Las cifras no pueden ser más desalentadoras: se estima que 1,2 millones de personas murieron como resultado de infecciones bacterianas resistentes a los antibióticos en 2019. Esto no solo es un completo desastre, sino también una curiosa historia que se encuentra entre el éxito y el fracaso.
Los antibióticos y su Edad de Oro
Al discutir el origen de los antibióticos, como explica Alfons, debemos retroceder más de 100 años a principios de la década de 1910, cuando se introdujo el primer agente antimicrobiano moderno. Se conocía como Salvarsan (arsfenamina o compuesto 606) y había sido descubierto por Paul Ehrlich. Fue el primer tratamiento eficaz para la sífilis y la tripanosomiasis africana. Este tratamiento inició una nueva era en la medicina.
Sin embargo, el mayor cambio tuvo lugar en 1928, cuando el científico escocés Alexander Fleming descubrió la penicilina. Esta nueva molécula pequeña supuso una gran revolución, no solo desde la perspectiva de la salud pública, sino también desde el punto de vista de la industria farmacéutica.
Desde una perspectiva de salud pública, la introducción y el uso generalizado de antibióticos en la década de 1940 tuvo un impacto extremadamente alto y las muertes causadas por enfermedades infecciosas se redujeron en un 70 %.
La penicilina también abrió una nueva era en la industria farmacéutica emergente y fue el primer paso en la Edad de Oro de los antibióticos, ejemplificada por Pfizer. La empresa fue fundada en 1849 como fabricante de medicamentos y proveedor de productos químicos finos. La empresa creció, pero el gran cambio se produjo gracias a los antibióticos. Primero, durante la Segunda Guerra Mundial, Pfizer (y otros proveedores de productos químicos) se convirtieron en los principales proveedores de penicilina para el Ejército Aliado. Después de la guerra, cuando el negocio declinó y el precio de la penicilina cayó, los científicos de Pfizer comenzaron a buscar nuevos antibióticos. El descubrimiento de la oxitetraciclina en 1950 transformó a la empresa de una empresa de productos químicos finos a una corporación farmacéutica basada en la investigación.
Este fue uno de los primeros disparos en la carrera de los antibióticos, y todas las compañías farmacéuticas siguieron los pasos de Pfizer, convirtiéndose en compañías farmacéuticas basadas en la investigación e invirtiendo para producir sus propios antibióticos nuevos. Este cambio, que fue respaldado por el marketing farmacéutico temprano, fue de gran escala. A modo de ejemplo, Pfizer tenía 8 vendedores en 1950 y había ampliado esta fuerza de ventas a 2000 personas en 1957.
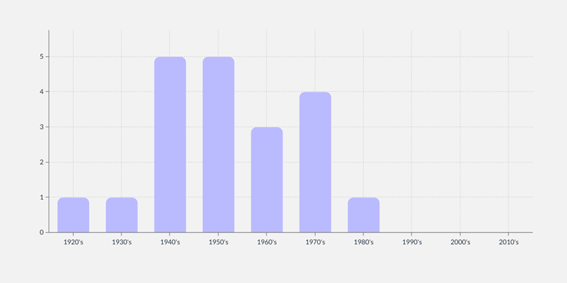
La mayoría de los antibióticos que conocemos y usamos fueron descubiertos durante esta Edad de Oro, pero esto comenzó a disminuir en la década de 1970 con el inicio del vacío de descubrimiento, que comenzó en la década de 1980 y todavía está con nosotros hoy. La nueva clase de antibiótico más reciente que se introdujo con éxito como tratamiento se descubrió en 1987 y se introdujo en 2003, hace casi 20 años.
La edad de oro de los antibióticos fue desde la década de 1940 hasta principios de la de 1970, cuando la mayoría de las nuevas clases de antibióticos se introdujeron en el uso clínico.
La resistencia a los antimicrobianos se cobrará 10 millones de muertes en 2050
Las consecuencias se resumen en el primer párrafo de esta revisión. Las muertes causadas por infecciones resistentes a los antimicrobianos van en aumento y, según el grupo interinstitucional de las Naciones Unidas sobre resistencia a los antimicrobianos, se prevé que aumenten a la increíble cantidad de 10 millones por año para 2050.
¿Qué ha sucedido para crear este cambio de una Edad de Oro a un desierto en menos de 50 años? La respuesta es rápida y fácil: el mercado. Aunque el mercado de los antibióticos fue un mercado increíblemente rentable desde la década de 1950 hasta principios de la de 1970, invertir en el descubrimiento y desarrollo de nuevos antibióticos ya no es un mercado rentable para las compañías farmacéuticas.
Solo es una cuestión de dinero
La inversión estimada involucrada en el desarrollo de un nuevo antibiótico fue de alrededor de US $ 1500 millones en 2017, mientras que las ventas estimadas de un nuevo antibiótico ascienden a US $ 46 millones por año. Las matemáticas básicas nos dicen que no hay margen económico para los nuevos antibióticos. Esto ha hecho que la mayoría de las empresas farmacéuticas abandonen el mercado de los antibióticos y se trasladen a áreas terapéuticas más rentables, como la oncología.
Un factor limitante adicional para el mercado de los antimicrobianos es que hay pocos inventos nuevos, aunque existen. Sin embargo, no se utilizan mucho debido a la preocupación por la resistencia. Los antibióticos nuevos no se usan como opción de tratamiento inicial porque los antibióticos más comunes se usan primero y los antibióticos nuevos se mantienen como tratamiento de segunda línea. Esta estrategia significa que los nuevos antibióticos están a salvo de generar resistencia antimicrobiana. Esto podría ser beneficioso para la salud mundial, ya que es vital para prevenir nuevas resistencias. Sin embargo, no es bueno desde el punto de vista económico y en consecuencia para la salud mundial (si no hay mercado no hay negocio y entonces no hay tratamientos). Si no se utilizan nuevos antibióticos, no se venden y, por lo tanto, el rendimiento de las inversiones durante el período protegido por patente es menor de lo esperado.
Ya estamos en plena travesía del desierto
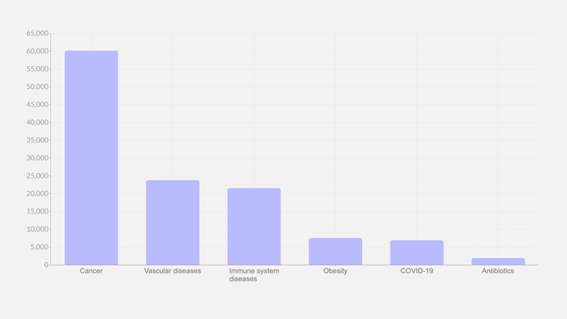
Este vacío de descubrimiento es claro si consideramos las aprobaciones de nuevos antibióticos. Solo se aprobaron 65 nuevos antibióticos entre 1980 y 2014, un número extremadamente bajo en comparación con los 125 nuevos medicamentos contra el cáncer aprobados en el mismo período. Si utilizamos los ensayos clínicos como referencia para el futuro, el panorama también es deprimente. Según Clinicaltrials.gov, se realizaron (o están en curso) un total de 297.813 ensayos clínicos entre el 1 de enero de 2010 y finales de 2021. Solo 1.991 estaban relacionados con antibióticos, mientras que hubo 60.238 para cáncer, 23.860 para enfermedades vasculares y 7.016 para COVID. -19 (¡en menos de dos años!).
La situación es desastrosa: los tratamientos actuales son cada vez menos efectivos, mientras que casi no tenemos soluciones en proyecto.
Los últimos once años, desde 2010 hasta finales de 2021, se realizaron un total de 297.813 ensayos clínicos, de ellos solo 1.991 relacionados con antibióticos.
Sin rentabilidad económica no hay investigación
En los últimos años, la mayoría de las principales compañías farmacéuticas han tirado la toalla en la investigación de antibióticos y han terminado con todas las líneas de investigación relacionadas con los antibióticos. Solo unas pocas compañías farmacéuticas importantes aún tienen líneas activas de investigación en antibióticos. Algunas empresas más pequeñas y organizaciones benéficas se están anticipando a este importante problema de salud mundial y han estado trabajando en la investigación de antibióticos. Algunos actores importantes no han logrado desempeñar un papel con sus propias iniciativas, como REPAIR de NovoHoldings y CARB-X de algunos gobiernos que trabajan con fundaciones públicas y organizaciones benéficas. Ambos programas comenzaron con muchas promesas, pero tanto los inversores directos como los accionistas promotores decidieron no invertir en el proyecto.
La lección del COVID-19
Algo ha cambiado en los últimos 2-3 años. El COVID-19 nos ha mostrado cómo una pandemia puede afectar la economía global y cómo un problema de salud puede conducir a resultados económicos desastrosos. La Federación Internacional de Fabricantes y Asociaciones Farmacéuticas anunció el Fondo de Acción AMR en julio de 2020. Se trata de un fondo de mil millones de dólares estadounidenses que esperaba proporcionar de 2 a 4 antibióticos nuevos para 2030. Este fondo involucra a 24 empresas importantes, incluidas NovoHoldings y Novartis, que había malas experiencias en las iniciativas REPAIR y CARB-X respectivamente.
Pero estas inyecciones de efectivo no resolverán el problema. ¿Qué pasará cuando el fondo llegue a su fin? ¿Qué pasará si no hay resultados de la iniciativa? Los antibióticos deben ser económicamente más viables sin la participación de organizaciones benéficas, y un modelo de suscripción podría ser una solución. Algunos proveedores de atención médica y fabricantes de medicamentos se están moviendo hacia este nuevo enfoque, en el que los antibióticos se pagan mediante una suscripción. Este enfoque, que actualmente se encuentra en sus primeras etapas en el Reino Unido, se basa en un pago inicial a los fabricantes de medicamentos para iniciar proyectos de investigación sobre antibióticos y pagos futuros para brindar tratamientos, que no están directamente relacionados con la cantidad de tratamientos brindados.
Este tipo de iniciativa, que esperamos estimule la investigación y el desarrollo de antibióticos, es muy bienvenida. Sin embargo, también son bienvenidas otras iniciativas anteriores y en curso, que llaman a la acción contra la resistencia a los antimicrobianos. Como ejemplo, uno de los proyectos más antiguos es el grupo ReAct, que se creó en 2005 como una de las primeras redes internacionales independientes que abogan y fomentan el compromiso mundial sobre la resistencia a los antibióticos. También existen iniciativas para concienciar a la población, de las cuales las más conocidas son la Semana Mundial de Concienciación sobre los Antimicrobianos, impulsada por la Organización Mundial de la Salud desde 2015, y el Día Europeo de Concienciación sobre los Antibióticos establecido en 2008, que se celebra lugar el 18 de noviembre.
La pandemia de COVID-19 ha llevado a un enfoque en esta patología global, pero también es una plataforma para estimular la investigación y el desarrollo de tratamientos antimicrobianos y antiinfecciosos en general. No solo las personas sino también los gobiernos son ahora más conscientes de los costos económicos, humanos y de salud de una pandemia.
The Hacking Bacteria’s Project
En DevsHealth, comenzamos nuestra propia iniciativa a fines del año pasado para combatir la resistencia a los antimicrobianos y lanzamos el proyecto Hacking Bacteria. Queremos trabajar para mejorar la salud mundial, pero conocemos nuestros límites. Con este proyecto, pretendemos asociarnos con otras empresas, universidades y centros de investigación para que nuestra tecnología esté disponible para hacer nuestra contribución en la lucha contra las bacterias resistentes a los medicamentos.
Todos debemos luchar juntos para detener el aumento de muertes por infecciones por resistencia a los antimicrobianos. Debemos comenzar a trabajar en nuevas investigaciones sobre antibióticos ahora, de lo contrario el Cisne Rojo será inevitable.